Características y Tipos del Stent Ultimaster™
Tema Especial
Nuevos conocimientos de MASTER DAPT
El subanálisis de PCI compleja de MASTER DAPT fue presentado en EuroPCR 2022. Descárguelo aquí.
Resultados de MASTER DAPT
Haga clic aquí para descargar un resumen de los criterios de valoración primarios del ensayo.
El BP-DES más estudiado, con más de 50,000 pacientes en todo el mundo
El BP-DES más estudiado, con más de 50,000 pacientes a nivel mundial1,2
Ultimaster™ ha sido evaluado a nivel global en estudios clínicos patrocinados por Terumo y en investigaciones independientes, incluyendo a más de 50,000 pacientes. Los programas clínicos han demostrado de manera constante la eficacia y seguridad de Ultimaster™, incluso en lesiones complejas.
| Número de pacientes | Diseño | Resultados primarios | Subestudio | |
|---|---|---|---|---|
| MASTER DAPT | 4300 | Estudio iniciado por investigadores, aleatorizado, comparación de DAPT corta vs estándar | NACE, MACCE, MCB a 11 meses (12 meses post-PCI índice) | En curso, protocolo publicado |
| e-Ultimaster | 37,198 | Estudio de un solo brazo, todos los pacientes, uso en práctica clínica real | TLF a 1 año | Completado y aceptado para publicación |
| CENTURY II | 1123 | Aleatorizado 1:1 vs Xience | Libertad de TLF a 9 meses | Publicado y completado |
| DISCOVERY 1TO3 | 60 | Estudio de un solo brazo, pacientes con enfermedad multivaso | Cobertura de struts evaluada por OFDI a 3 meses | Publicado y completado |
| MODEL U-SES | 1,695 | Registro prospectivo multicéntrico, estudio de un solo brazo iniciado por investigadores | Criterio de valoración compuesto de muerte por cualquier causa, infarto de miocardio, accidente cerebrovascular, trombosis del stent definitiva/probable según ARC y BARC 3 o 5 durante los 12 meses posteriores a la colocación del stent | Publicado y completado |
| SCAAR | 3,253 | Registro multicéntrico en Suecia | ST, tasa de reestenosis | En curso |
| SCC registry | 1,727 | Estudio de un solo brazo, todos los pacientes, estudio de un solo centro | TLR, TLF, MACE | Publicado y completado |
| ULISS | 1,660 | Estudio de un solo brazo, todos los pacientes, estudio de un solo centro | TLR, TLF, criterio de valoración compuesto de muerte cardíaca, TV-MI | Publicado y completado |
| MASTER | 500 | Aleatorizado 3:1 vs BMS en pacientes con STEMI | Seguridad a 1 mes, eficacia a 6 meses, seguridad y eficacia a 12 meses | Publicado y completado |
| COLOR | 388 | Ensayo iniciado por investigadores, aleatorizado, PCI compleja de acceso radial de gran calibre | Hemorragia BARC o complicaciones vasculares relacionadas con el sitio de acceso | En curso |
| CENTURY | 105 | Estudio de un solo brazo, first-in-man | Pérdida tardía a 6 meses | Publicado y completado |
| CENTURY JSV | 70 | Estudio de un solo brazo, pacientes que requieren stents de 2.25 mm de diámetro | Libertad de MACE a 9 meses | Publicado y completado |
| TCD-10023PK | 22 | Estudio de un solo brazo, farmacocinética | Concentración de sirolimus en muestras de sangre periférica a los 28 días post-implante de Ultimaster™ | Publicado y completado |
Ver más sobre la evidencia clínica
El registro más grande de BP-DES en el mundo real demuestra un desempeño clínico favorable3
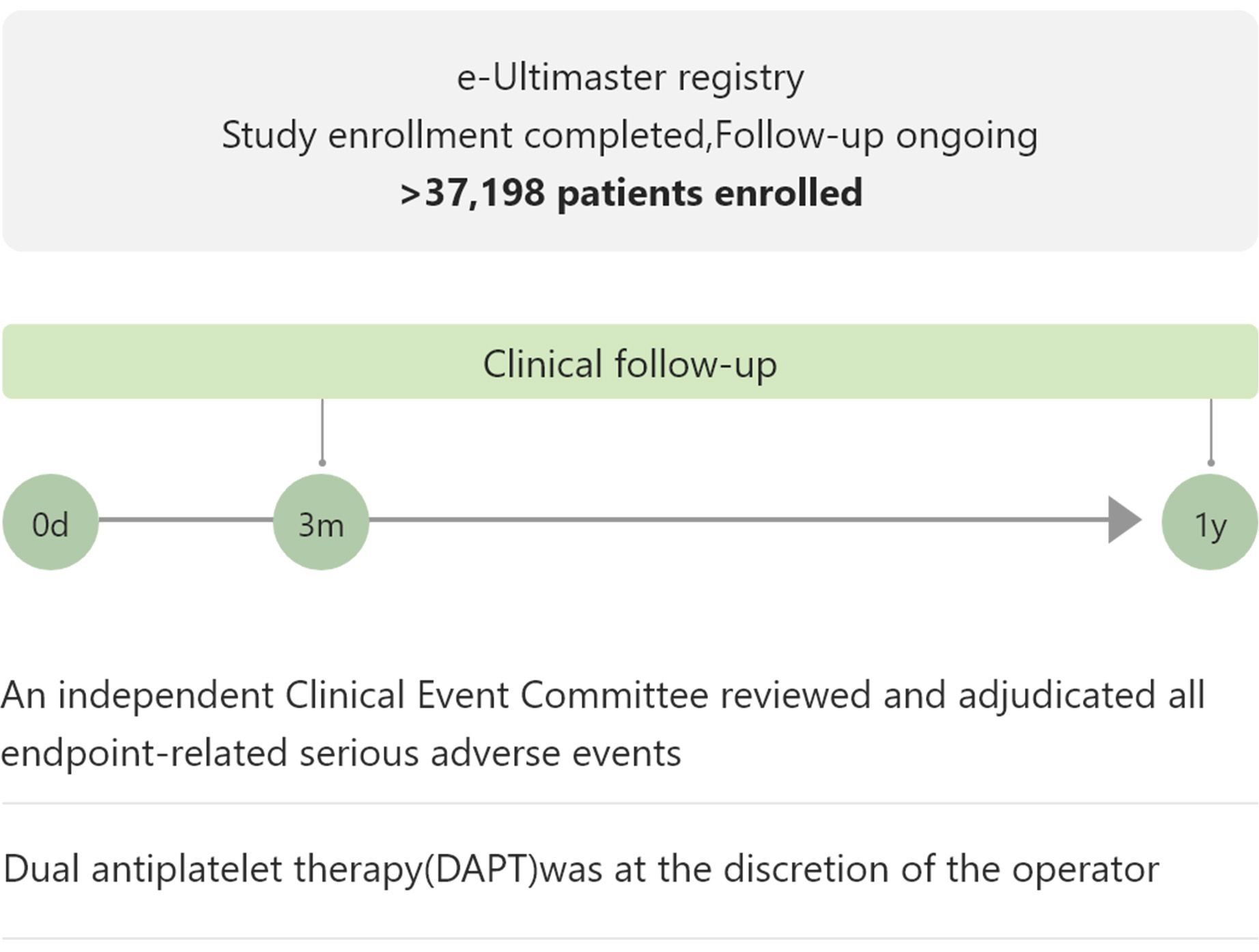
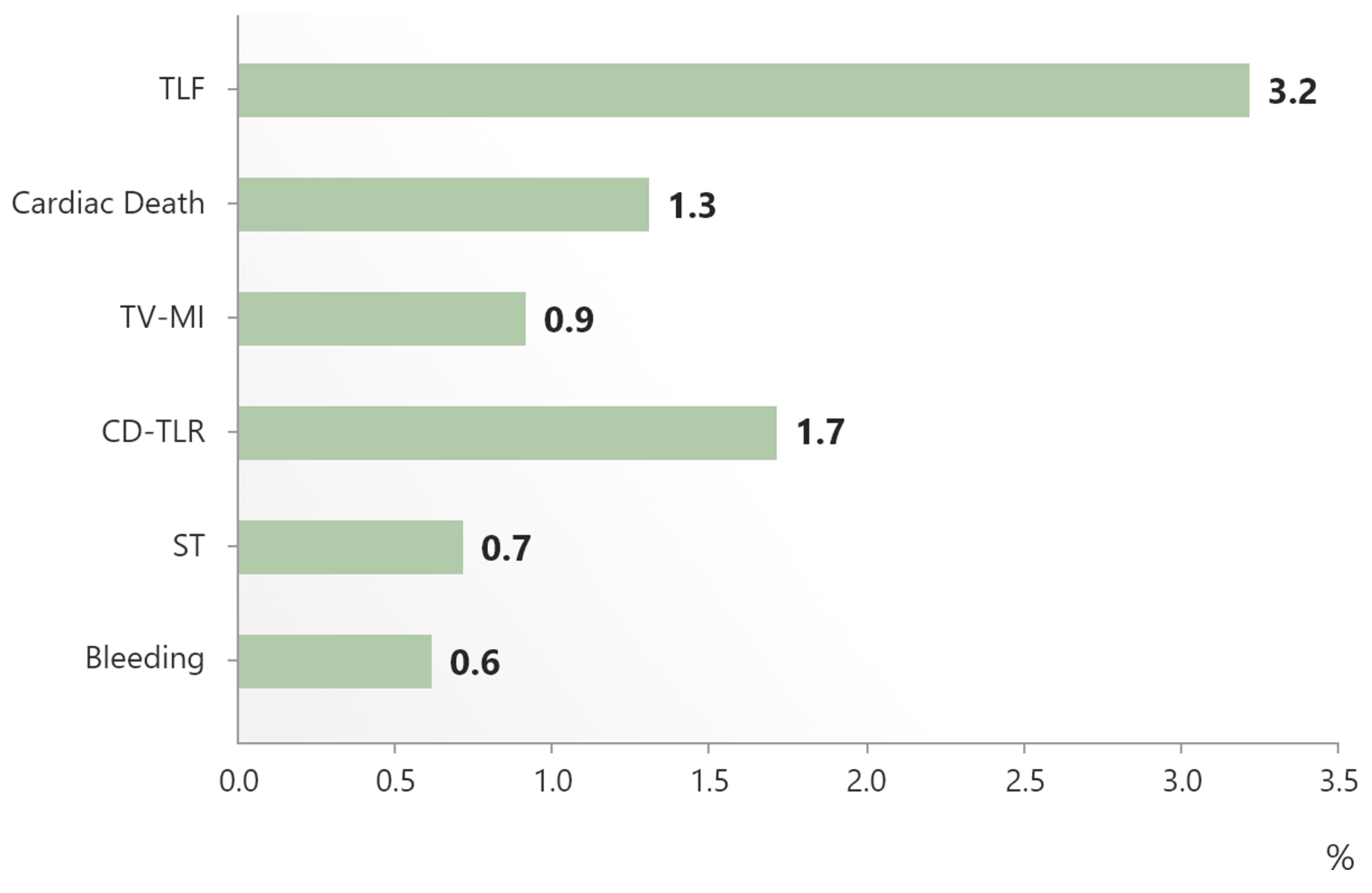
Obtenga más información sobre e-Ultimaster
La empresa con mayor trayectoria en BP-DES4

Buena fuerza de transmisión incluso cuando el catéter guía no proporciona suficiente soporte1
Ultimaster™ está diseñado para facilitar la entrega en TRI. En TRI, el catéter guía en ocasiones no proporciona un soporte de respaldo suficiente, lo que puede llevar a la desinserción del catéter guía en el tratamiento de lesiones complejas. Ultimaster™ no solo respalda la entrega en casos desafiantes, sino también la atención pensada para sus pacientes.
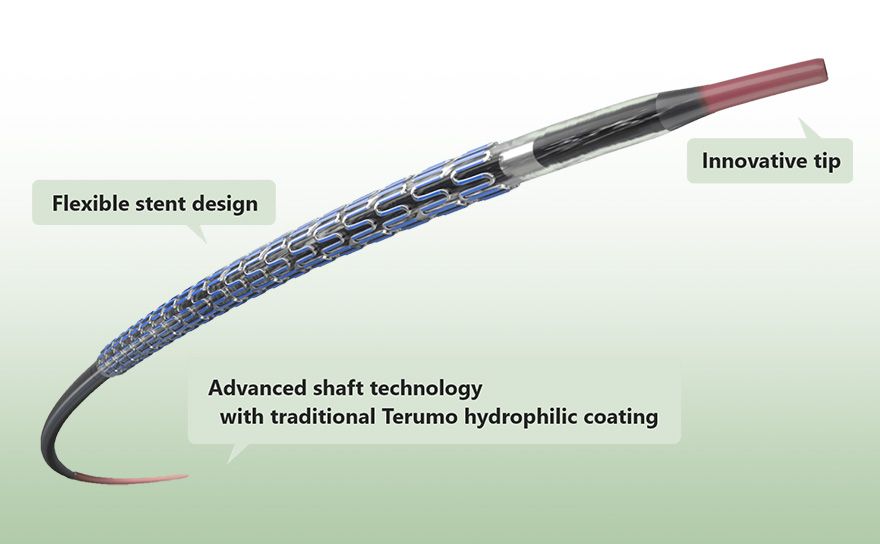
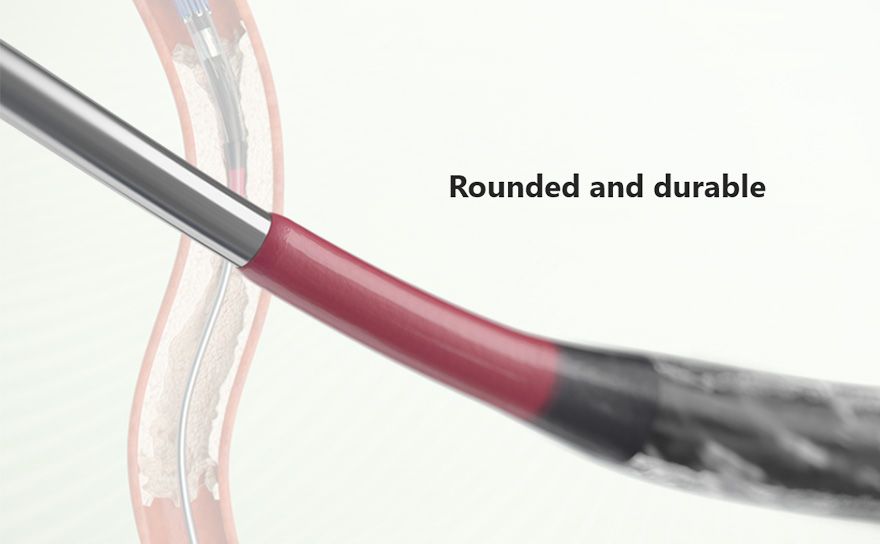

Tecnología de eje avanzada con la tecnología tradicional de Terumo
Ultimaster™ fue desarrollado aplicando tanto la tecnología avanzada utilizada para el eje del balón PTCA de Terumo como la tecnología tradicional de recubrimiento hidrofílico utilizada para la guía de Terumo. Estas tecnologías mejoran la empujabilidad y la capacidad de seguimiento en condiciones desafiantes como TRI donde el soporte de respaldo de un catéter guía es limitado.


Conozca más sobre nuestro producto
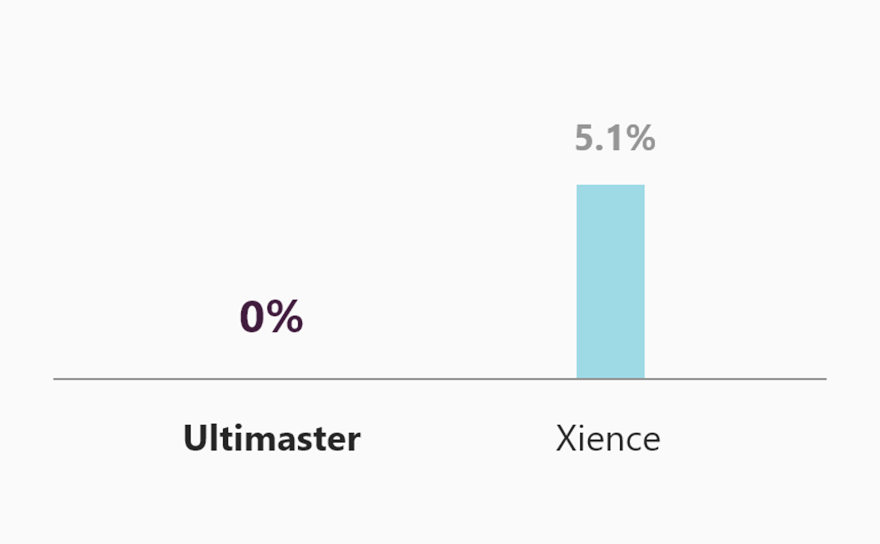
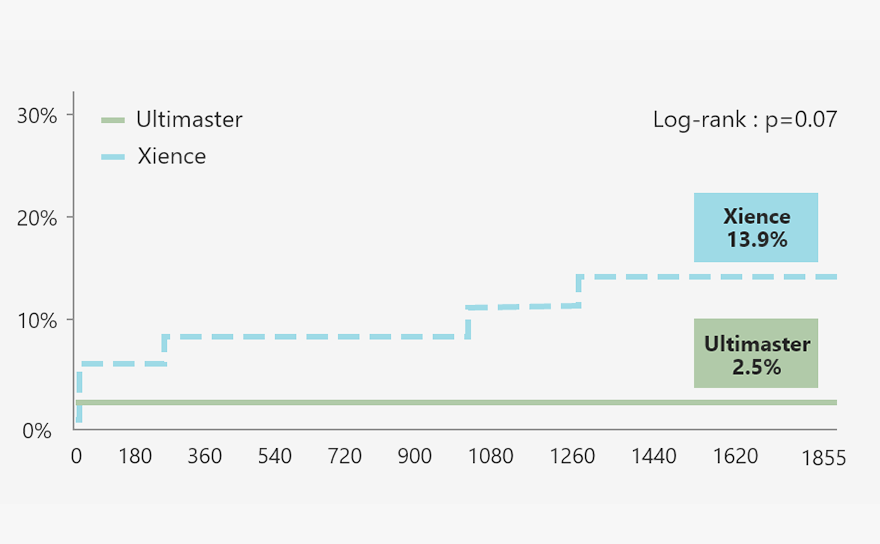
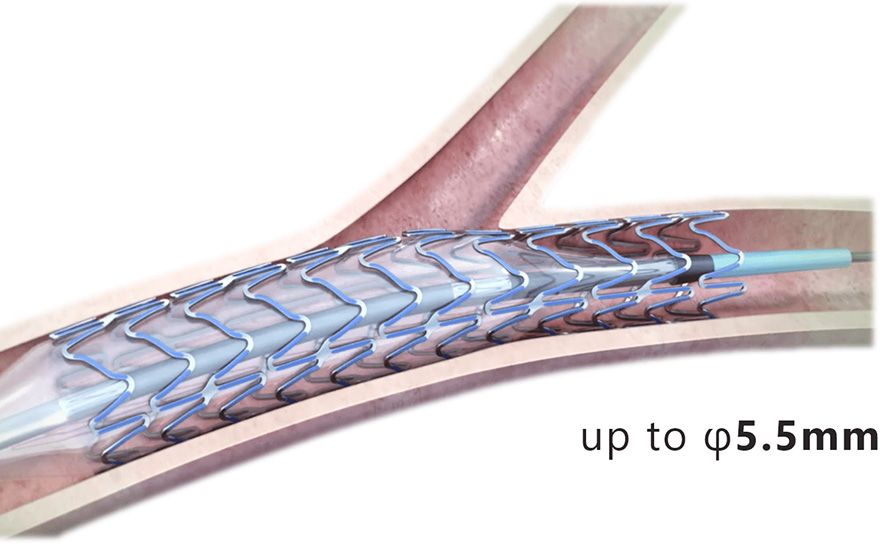
Mayor rango de sobreexpansión
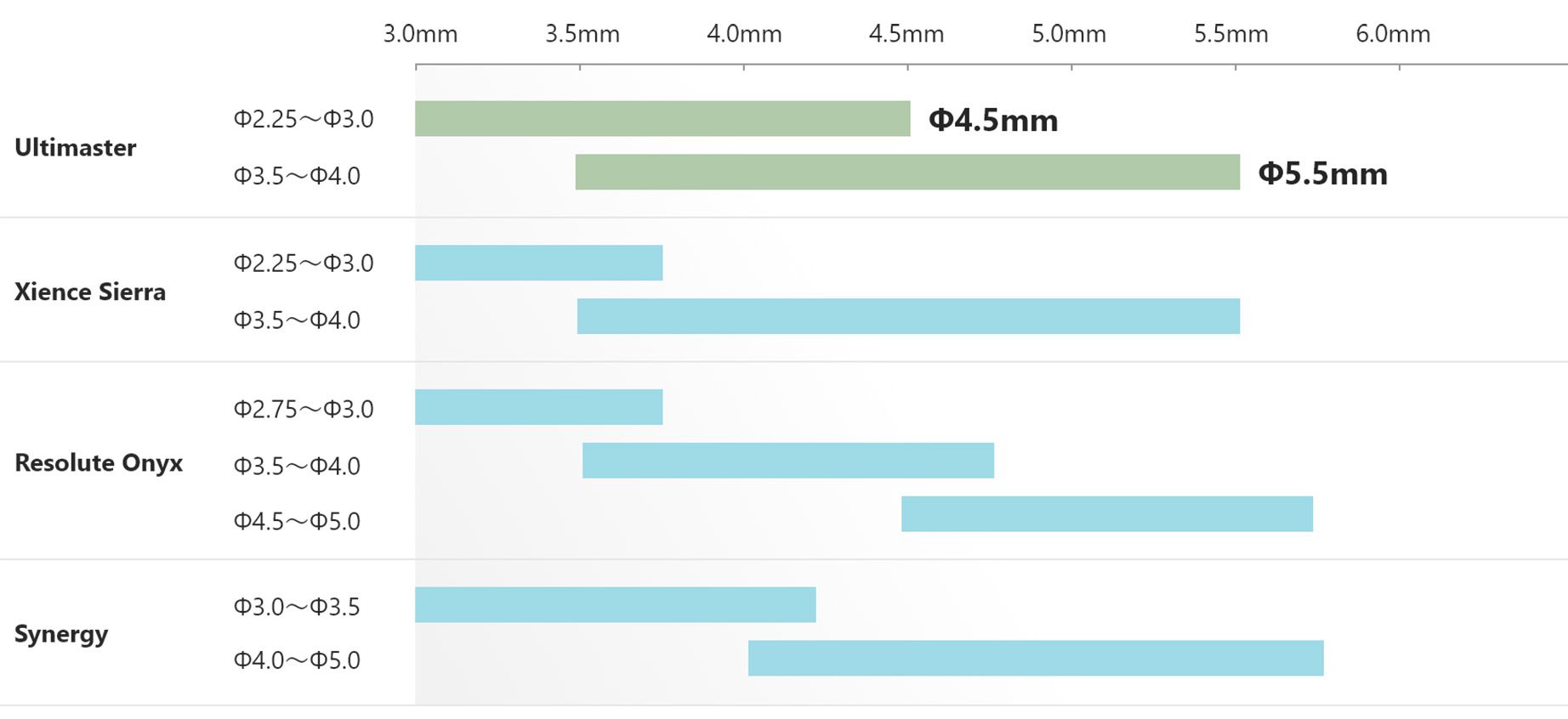
| Diseño de stent para Φ4.0mm | Ultimaster™ | Synergy | Xience Sierra | Resolute Onyx |
|---|---|---|---|---|
| Diseño de Stent | 
| 
| 
| 
|
| Longitud total de la corona medida | 21.5mm | 19.8mm | 20.1mm | 15.2mm |
Acceso suave a la rama lateral gracias al diseño con el tamaño de celda abierta más grande
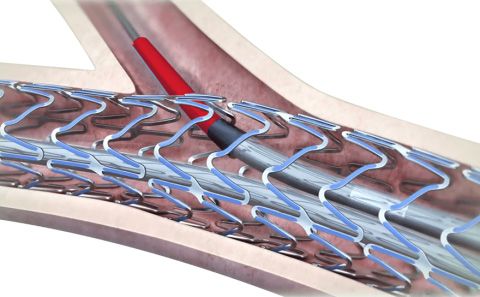
| Diseño de stent para Φ4.0mm | Ultimaster™ | Synergy | Xience Sierra | Resolute Onyx |
|---|---|---|---|---|
| Diseño de Stent | 
| 
| 
| 
|
| Longitud total de la corona medida | 21.5mm | 19.8mm | 20.1mm | 15.2mm |
| Diámetro Máximo de Celda | 6.8mm | 5.7mm | 4.8mm | 6.5mm |
| Área Máxima de Celda | 36.3mm2 | 25.7mm2 | 18.1mm2 | 33.2mm2 |
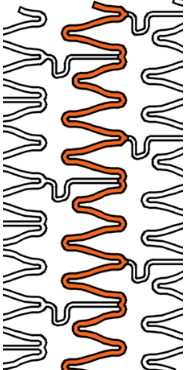
Tecnología de recubrimiento con gradiente abluminal que garantiza la integridad del polímero
Nuestros productos se fabrican prestando atención a los detalles. No hay recubrimiento de fármaco en la plataforma del stent en el que se concentre una gran tensión cuando el stent se sobreexpande. Ultimaster™ mantiene la integridad del polímero incluso cuando el stent se expande hasta el diámetro máximo.






